アスコルビン酸
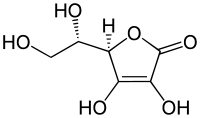
アスコルビン酸(アスコルビンさん、英: ascorbic acid)は、栄養素のビタミンCとしてはたらく、ラクトン構造を持つ有機化合物の1種である。光学活性化合物であり、ビタミンCとして知られるのはL体の方である。食品添加物の酸化防止剤として、広く使用される。IUPAC命名法では、フランの誘導体と見なして、(R)-3,4-ジヒドロキシ-5-((S)-1,2-ジヒドロキシエチル)フラン-2(5H)-オンと表される。
| アスコルビン酸 | |
|---|---|
| |

| |
(R)-3,4-ジヒドロキシ-5-((S)- 1,2-ジヒドロキシエチル)フラン-2(5H)-オン | |
別称 ビタミンC | |
| 識別情報 | |
| CAS登録番号 | 50-81-7 |
| PubChem | 5785 |
| J-GLOBAL ID | 200907081023027887 |
| EC番号 | 200-066-2 |
| E番号 | E300 (酸化防止剤およびpH調整剤) |
| KEGG | D00018 |
| |
| |
| 特性 | |
| 分子式 | C6H8O6 |
| モル質量 | 176.1241 g/mol |
| 外観 | 白色または淡黄色の固体 |
| 密度 | 1.65 g/cm3 |
| 融点 |
190-192 °C, 463-465 K, 374-378 °F (分解) |
| 水への溶解度 | 33g/100ml |
| エタノールへの溶解度 | 2g/100ml |
| グリセロールへの溶解度 | 1g/100ml |
| プロピレングリコールへの溶解度 | 5g/100ml |
| 酸解離定数 pKa | 4.17(1段階)11.6(2段階) |
| 危険性 | |
| 安全データシート(外部リンク) | ScienceLab.com |
| 半数致死量 LD50 | 11.9 g/kg(経口、ラット)[1] |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
工業的製造法
編集L-アスコルビン酸はグルコースを原料として、主に2通りの経路で製造される。1930年代に開発された ライヒシュタイン法では、1段階の発酵のあとに、化学合成へ移る。より新しい2段階発酵法は、もとは1960年代に中国で開発された方法であるが、そこではその化学合成の後ろのほうの段階も酵素反応で置き換えている。どちらの経路も、用いたグルコースから約60%の収率でアスコルビン酸を産出する。全世界におけるアスコルビン酸の年間の生産量は約110,000トンにのぼる[いつ?]。
化学的性質
編集酸性
編集アスコルビン酸はビニル性カルボン酸のように振る舞い、二重結合のπ電子がヒドロキシ基とカルボニル基の間に伝わることにより高い酸性を示す (pKa1 = 4.17、pH = 2 (50 mg/mL))。これは、プロトンを放出した後の共役塩基が共鳴構造を持ち、負電荷を非局在化させて安定化できるためである。
アスコルビン酸は還元性を示す。適当な酸化剤(空気中の酸素およびハロゲンなど)の作用により、プロトンを2個放出してデヒドロアスコルビン酸に変わる。この性質により、酸化防止剤として用いられる。
酸化
編集アスコルビン酸イオンは、典型的な生物学的pH値における優勢種である。 マイルドな還元剤及び抗酸化物質 (酸化防止剤)である。 酸化で1番目の電子が失われることによりラジカルカチオンが形成され、次に2番目の電子が失われることによりデヒドロアスコルビン酸が形成される。 通常、ヒドロキシルラジカルなどの活性酸素種の酸化剤と反応する。
アスコルビン酸は、セミデヒドロアスコルビン酸と呼ばれるそれ自体のラジカルイオンの共鳴安定化された性質により、単一の電子を転送することができるという特質をもつ。 化学反応式は以下のとおり:
- RO• + C6H7O−
6 → RO− + C6H7O•
6 → ROH + C6H6O6
酸素にさらされると、アスコルビン酸はさらに酸化分解されて、ジケトグロン酸、キシロン酸、トレオン酸、シュウ酸などのさまざまな生成物になる。
活性酸素種は、核酸、タンパク質、脂質との相互作用の可能性があるため、分子レベルで動植物に損傷を与えるものであり、これらのラジカルが連鎖反応を開始することがある。 アスコルビン酸塩は、電子移動反応によってこれらの連鎖ラジカル反応を終わらせることができる。 アスコルビン酸塩の酸化型は比較的非反応性であり、細胞の損傷を引き起こさない。
しかしながら、アスコルビン酸塩は優れた電子供与体であるので、遊離金属イオンの存在下での過剰なアスコルビン酸塩は、フリーラジカル反応を促進するだけでなく開始することもできるため、特定の代謝状況において潜在的に危険な酸化促進化合物になり得る。
アスコルビン酸とアスコルビン酸ナトリウム、アスコルビン酸カリウム、アスコルビン酸カルシウム塩、アスコルビン酸グルコシドは、食品添加物である酸化防止剤として一般的に使用されている。 ただし、これらの化合物は水溶性であるため、脂肪を酸化から保護することはできない。この目的のために、アスコルビン酸と長鎖脂肪酸の脂溶性エステル(パルミチン酸アスコルビルまたはステアリン酸アスコルビル)を食品の抗酸化剤として使用することができる。
なお食品が、その加工中や保存中などに、その色が褐変する事を防止するために、アスコルビン酸自身が酸化されて、食品の側を還元する作用を利用する方法もある[2][注釈 1]。
互変異性
編集アスコルビン酸はプロトンの移動によって不安定なジケトンに互変異性する。この場合、エノール側が優勢である。エノールがプロトンを失うと、その二重結合からπ電子を受け取り、ジケトンが生成する。この互変異性では1,2-ジケトンと1,3-ジケトンが生成可能である。
定量法
編集アスコルビン酸の定量分析は、酸化還元滴定により行える。試料をメタリン酸水溶液に溶かし 0.05 mol/L ヨウ素溶液で滴定する。指示薬は、デンプン試液を用いる。この方法の中で、ヨウ素は酸化剤としてはたらく。
その他
編集ドイツ連邦リスク評価研究所 (BfR) の報告によれば、清涼飲料水中に安息香酸とアスコルビン酸が共存する場合には微量のベンゼンが生成する可能性があり、生成量は pH、温度、他の不純物(主に金属イオンが影響するものと思われる)、紫外線の影響を受けると言う[3][4]。
アスコルビン酸の構造を決定したウォルター・ハースは、1937年にノーベル賞を受賞した。
アスコルビン酸の名前の由来は、壊血病 (scurvy) の治療に効果があったことによる【a(否定)+ scorbutic(壊血病に罹った)】。
脚注
編集注釈
編集- ^ ただし、食品の褐変を防止する方法は、1つだけではない。例えば、クエン酸の場合は、クエン酸が金属イオンを捕えて食品の褐変を防いでいるのであって、アスコルビン酸とは機序が異なる。もちろん、例えば果皮を剥いたリンゴの褐変を防止するために食塩水を用いた場合は、リンゴが持つポリフェノールオキシターゼの作用を食塩水が阻害する事を利用して褐変を防いでいるのであって、やはり全く機序が異なる。
出典
編集- ^ “Safety (MSDS) data for ascorbic acid”. オックスフォード大学 (2005年10月9日). 2007年2月21日閲覧。
- ^ 日本海水学会(編)『塩のことば辞典』 p.89(「褐変防止」の項目) 素朴社 2007年6月10日発行 ISBN 978-4-903773-03-2
- ^ BfRによる原著文献(ドイツ語) (PDF)
- ^ P30に国立医薬品食品衛生研究所安全情報部による日本語の摘要 (PDF)