ヤップ・クリンゲマン反応
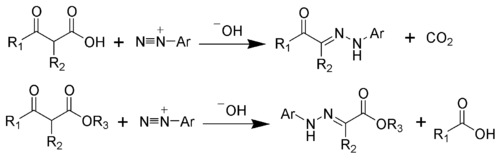
ヤップ・クリンゲマン反応(ヤップ・クリンゲマンはんのう、英語: Japp–Klingemann reaction)とは、有機化学における人名反応のひとつ。活性メチン化合物から塩基により発生させたカルバニオンが芳香族ジアゾニウム化合物と縮合してヒドラゾンとなる反応のこと(下式)[1]。縮合するにあたってカルボン酸または二酸化炭素が脱離する。1887年に、フランシス・ロバート・ヤップと フェリックス・クリンゲマン により報告された[2][3][4][5][6]。
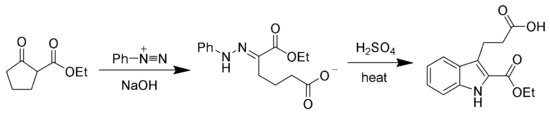
ヤップ・クリンゲマン反応の生成物であるヒドラゾン誘導体は、より複雑な有機分子への合成中間体として用いられる。例えば、アリールヒドラゾンを強酸のもとに加熱するとフィッシャーのインドール合成の経路によりインドール環が得られる[7][8][9]。
反応機構
編集エステルを基質とするヤップ・クリンゲマン反応の機構は下式のように考えられている[1]。まず塩基により活性メチン化合物 1 からプロトンが引き抜かれ、カルバニオン 2 が生じる。これがジアゾニウムイオンとカップリングを起こし、アゾ化合物 3 となる。実際にアゾ化合物が単離された例がある。多くの場合では 3 は四面体型中間体 4 を経て速やかに分解しアニオン 5 とカルボン酸 6 となり、プロトンを受け渡した後にヒドラゾン 7 が生じる。
参考文献
編集- ^ a b 総説: Phillips, R. R. Org. React. 1959, 10, 143-178.
- ^ Japp, F. R.; Klingemann, F. Ber. Deutsch. Chem. Ges. 1887, 20, 2942–2944. DOI: 10.1002/cber.188702002165
- ^ Japp, F. R.; Klingemann, F. Ber. Deutsch. Chem. Ges. 1887, 20, 3284–3286. DOI: 10.1002/cber.188702002234
- ^ Japp, F. R.; Klingemann, F. Ber. Deutsch. Chem. Ges. 1887, 20, 3398–3401. DOI: 10.1002/cber.188702002268
- ^ Japp, F. R.; Klingemann, F. Liebig Ann. Chem. 1888, 247, 190–225. DOI: 10.1002/jlac.18882470208
- ^ 実施例: Reynolds, G. A.; VanAllan, J. A. Organic Syntheses, Coll. Vol. 4, p.633 (1963); Vol. 32, p.84 (1952). オンライン版
- ^ Robinson, B. Chem. Rev. 1969, 69, 227-250. 10.1021/cr60258a004
- ^ Bowman, R. E.; Goodburn, T. G.; Reynolds, A. A. J. Chem. Soc., Perkins Trans 1 1972, 1121-1123. DOI: 10.1039/P19720001121
- ^ Meyer, M. D.; Kruse, L. I. J. Org. Chem. 1984, 49, 3195-3199. DOi: 10.1021/jo00191a028