イプラグリフロジン
(スーグラから転送)
イプラグリフロジン(Ipragliflozin、開発コード:ASP1941)は2型糖尿病治療薬の一つである。SGLT2阻害薬の一番手である。商品名はスーグラ。(アステラス製薬販売、寿製薬コ・プロモーション、MSDコ・プロモーション)日本では2014年1月17日製造承認、2014年4月17日に販売開始された[1]。
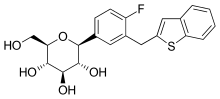 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | スーグラ |
| 法的規制 |
|
| データベースID | |
| PubChem | CID: 10453870 |
| ChemSpider | 8629286 |
| KEGG | D10196 |
| ChEMBL | CHEMBL2018096 |
| 化学的データ | |
| 化学式 | C21H21FO5S |
| 分子量 | 404.45 g/mol |
| |
| |
適応
編集- 2型糖尿病、1型糖尿病
作用機序
編集SGLT(英: Sodium-Glucose Co-Transporter: ナトリウム依存性グルコース輸送担体)は、細胞表面に存在する膜タンパク質で、ナトリウムとブドウ糖の細胞内への共輸送をつかさどっている。SGLT-2は、SGLTのサブタイプの一つで腎臓近位尿細管に多く存在し、ブドウ糖の尿中からの再取り込みにおいて重要な役割を担っている(SGLT-1は小腸粘膜に多く存在し、食事からのブドウ糖の吸収を担っている)。イプラグリフロジンはこのSGLT-2を選択的に阻害することで、ナトリウムとブドウ糖の原尿中からの再取り込みを抑制し、ブドウ糖の尿中排泄を促進することで、血糖値を低下させる。インスリン非依存性に血糖降下作用を発揮し、高インスリン血症を来さないため、インスリンの直接作用による副作用(低血糖、体重増加など)が発現しにくいことが期待されている。
臨床試験
編集副作用
編集承認時までの臨床試験では32.9%に副作用が認められた。主な副作用は頻尿8.9%、口渇4.3%、便秘3.2%、尿中β2ミクログロブリン増加2.5%、体重減少2.3%であった。
重大な副作用とされているものは、低血糖、腎盂腎炎(0.1%)、敗血症、脱水、ケトアシドーシスである[2]。血糖コントロールが良好でも脂肪酸代謝が亢進するのでケトアシドーシスが発生する可能性がある。
出典
編集- ^ スーグラ:日本初のSGLT-2阻害薬
- ^ “スーグラ錠25mg/スーグラ錠50mg 添付文書 2022年 8月改訂 ( 第3版 )”. 独立行政法人医薬品医療機器総合機構 (2022年8月). 2023年7月19日時点のオリジナルよりアーカイブ。2023年7月19日閲覧。